鳥類の検出ツールとしての環境DNAの可能性を実証
Demonstration of the potential of environmental DNA as a tool for the detection of avian species
- 掲載誌: Scientific Reports (2018)
- DOI: 10.1038/s41598-018-22817-5
はじめに
本研究は、鳥類の環境DNA (eDNA) を水試料から検出できるかを検証し、鳥類の検出に適したユニバーサルプライマー MiBird-U を設計・評価した論文です。 魚類・哺乳類向けの MiFish/MiMammal を基盤に 12S rRNA 領域(約 171 bp)を増幅するよう改良し、in silicoによる評価、22 種の組織 DNA による増幅試験、動物園の飼育ケージ水と野外池の水での実験を組み合わせて検証しています。 結果として、MiBird-U は鳥類に対して高い一致率を示し、動物園ケージ水では既知の対象種をすべて検出し、野外池でも複数の野鳥を検出しました。 本研究は、視認調査が難しい状況での鳥類多様性把握に eDNA メタバーコーディングが有効であることを示しています。
Introduction
鳥類は送粉や種子散布、昆虫食による植生保全など、陸域生態系の機能維持に深く関与しています。 一方で、都市化や森林分断などの人為的影響により鳥類群集の多様性が低下しつつあることが報告されています。 従来の視認調査は有効な手法ですが、夜間や森林内部の視界不良、調査者の同定スキル差といった制約も存在します。 そこで本研究では、鳥類が水辺で頻繁に水と接触するという生態的前提を活かし、水試料から鳥類の環境DNAを検出する手法が実用的かを検証しています。
Methods
プライマー設計と in silicoによる評価
プライマー設計では RefSeq から取得した鳥類 410 配列(2015-06-09)を用い、Mesquite で保存的領域の塩基組成を確認しながら設計しました。 3’末端には G/C を含めるが連続する G/C を避ける、テンプレートが C/T の場合は G を選ぶ、A/G の場合は T を選ぶといった設計指針を採用し、GC 含量は 40-60% とし、Tm は近似値になるよう OligoCalc で調整しています。 対象領域は 12S rRNA の挿入長約 171 bp で、MiFish/MiMammal を改変した MiBird-U (U = universal) として設計しました。MiSeq 用アダプタとランダム塩基を付与したプライマー配列は Table 1 にまとめています。
Table 1. MiBird プライマー配列(5’->3’)
| PCR | Primer name | Sequence |
|---|---|---|
| 1st PCR | MiBird-U-F | ACACTCTTTCCCTACACGACGCTCTTCCGATCT NNNNNN GGGTTGGTAAATCTTGTGCCAGC |
| 1st PCR | MiBird-U-R | GTGACTGGAGTTCAGACGTGTGCTCTTCCGATCT NNNNNN CATAGTGGGGTATCTAATCCCAGTTTG |
| 2nd PCR | 2nd PCR-F | AATGATACGGCGACCACCGAGATCTACAC XXXXXXXX ACACTCTTTCCCTACACGACGCTCTTCCGATCT |
| 2nd PCR | 2nd PCR-R | CAAGCAGAAGACGGCATACGAGAT XXXXXXXX GTGACTGGAGTTCAGACGTGTGCTCTTCCGATCT |
NNNNNN はランダム塩基、XXXXXXXX はインデックス配列。
設計したプライマーの結合性は、鳥類 410 配列に加えて、哺乳類 741 配列、両生類 197 配列、爬虫類 245 配列を対象に Ruby/Python のカスタムスクリプトでミスマッチ数を算出しました。 また、プライマー領域欠失を含むHemignathus munroi、Loxops coccineus、Arborophila rufipectus を除外した 407 配列について、種間編集距離を算出し、種判別に十分な多型が含まれるかを評価しました。 さらに primerTree (R 3.3.1) を用いて in silico PCR、配列取得、系統樹再構築までを行い、増幅可能な分類群の広がりを可視化しています。
組織DNAの増幅試験
鳥類 22 種の組織 DNA を抽出し、NanoDrop Lite で濃度測定後 15 ng/µL に希釈しました。PCR は 15 µL 反応系(滅菌蒸留水 4.5 µL、2× Gflex PCR Buffer 7.5 µL、各プライマー 0.7 µL(5 µM)、Tks Gflex DNA Polymerase 0.3 µL、テンプレート 1.2 µL)で実施しています。
PCR 条件の詳細は下表の通りです。
| 項目 | 条件 |
|---|---|
| 初期変性 | 94°C 1 分 |
| 変性 | 98°C 10 秒 |
| アニーリング | 50°C 10 秒 |
| 伸長 | 68°C 10 秒 |
| サイクル数 | 30 |
| 最終伸長 | 68°C 7 分 |
対象種とアクセッション番号は Table 2 に整理しました。
Table 2. 増幅試験に用いた鳥類組織DNA(22種)
| Common name | Scientific name | Accession No. |
|---|---|---|
| Spot-billed duck | Anas zonorhyncha | LC104767 |
| Grey nightjar | Caprimulgus indicus | LC104768 |
| Ancient murrelet | Synthliboramphus antiquus | LC104769 |
| Lesser sand plover | Charadrius mongolus | LC104770 |
| Oriental turtle dove | Streptopelia orientalis stimpsoni | LC104771 |
| Lesser cuckoo | Cuculus poliocephalus poliocephalus | LC104772 |
| Northern goshawk | Accipiter gentilis fujiyamae | LC104773 |
| Common kestrel | Falco tinnunculus | LC104774 |
| Chinese bamboo partridge | Bambusicola thoracicus | LC104775 |
| Red-throated loon | Gavia stellata | LC104776 |
| Red-crowned crane | Grus japonensis | LC104777 |
| Jungle crow | Corvus macrorhynchos | LC104778 |
| Eurasian sparrow | Passer montanus | LC104779 |
| Black-crowned night heron | Nycticorax nycticorax | LC104780 |
| Great white pelican | Pelecanus onocrotalus | LC104781 |
| Great cormorant | Phalacrocorax carbo hanedae | LC104782 |
| Japanese pygmy woodpecker | Dendrocopos kizuki | LC104783 |
| Little grebe | Tachybaptus ruficollis | LC104784, LC104785 |
| White-chinned petrel | Procellaria aequinoctialis | LC104786 |
| Short-tailed shearwater | Puffinus tenuirostris | LC104787 |
| King penguin | Aptenodytes patagonicus | LC104788 |
| Humboldt penguin | Spheniscus humboldti | LC327059 |
動物園および野外の池での採水
動物園での実験は、横浜市立よこはま動物園ズーラシアで 2016-12-13 に実施され、13 ケージ・16 種の飼育鳥を対象に採水しました(Table 3)。
Table 3. 動物園実験の対象鳥類(16種)
| Common name | Scientific name | Order | Family |
|---|---|---|---|
| Steller’s sea eagle | Haliaeetus pelagicus | Accipitriformes | Accipitridae |
| Black-tailed gull | Larus crassirostris | Charadriiformes | Laridae |
| Capercaillie | Tetrao urogallus | Galliformes | Tetraonidae |
| Lady Amherst’s pheasant | Chrysolophus amherstiae | Galliformes | Phasianidae |
| Ruddy shelducka | Tadorna ferruginea | Anseriformes | Anatidae |
| Temminck’s tragopan | Tragopan temminckii | Galliformes | Phasianidae |
| Victoria crowned pigeon | Goura victoria | Columbiformes | Columbidae |
| Mandarin duck | Aix galericulata | Anseriformes | Anatidae |
| Humboldt penguin | Spheniscus humboldti | Sphenisciformes | Spheniscidae |
| Snowy owl | Bubo scandiacus | Strigiformes | Strigidae |
| Oriental white stork | Ciconia boyciana | Ciconiiformes | Ciconiidae |
| White-naped crane | Grus vipio | Gruiformes | Gruidae |
| Common crane | Grus grus | Gruiformes | Gruidae |
| Southern ground hornbill | Bucorvus leadbeateri | Coraciiformes | Bucerotidae |
| Harris’s hawk | Parabuteo unicinctus | Accipitriformes | Accipitridae |
| Emu | Dromaius novaehollandiae | Struthioniformes | Casuariidae |
a: 複数種が同居する通り抜けケージで飼育。
うち Ruddy shelduck は複数種が混在する通り抜けケージで飼育され、同一ケージ内の複数種が同時に検出される設計になっています。 各ケージの水 100-200 mL を 0.45 µm Sterivex で濾過し、RNAlater を約 2 mL 注入して 4°C で保管し、採水操作の陰性対照として蒸留水 3 例を持参しました。 また、未知組成の環境試料として千葉市の船田池からも同様の手順で採水しています。
DNA抽出、ライブラリ調製、シーケンス
Sterivex フィルターから DNeasy Blood and Tissue Kit を用いて DNA を抽出し、RNAlater 除去後に Proteinase-K 20 µL、PBS 220 µL、Buffer AL 200 µL を混合した 440 µL を添加し、50°C で 20 分の回転インキュベーションで溶菌した上で精製し、最終的に 100 µL で溶出しました。ライブラリ調製は前後工程を分離した環境下で実施し、PCR ネガティブコントロールを 2 サンプル設けています。
インデックスを付与した後、AMPure XP で精製し、約 370 bp を E-Gel SizeSelect でサイズ選択、Qubit で定量して 4 nM に調整し、MiSeq Nano v2 (2 × 150 bp) でシーケンスしています。
1st PCR の条件は下記の通りです。総反応液量は 12 µL です。
| 項目 | 条件 |
|---|---|
| 2× KAPA HiFi HotStart ReadyMix | 6.0 µL |
| MiBird primer-F | 0.7 µL |
| MiBird primer-R | 0.7 µL |
| DDW | 2.6 µL |
| PCR template | 2.0 µL |
| 項目 | 温度 | 時間 | サイクル |
|---|---|---|---|
| 初期変性 | 95°C | 3 分 | 1 |
| 変性 | 98°C | 20 秒 | 35 |
| アニーリング | 65°C | 15 秒 | 35 |
| 伸長 | 72°C | 15 秒 | 35 |
| 最終伸長 | 72°C | 5 分 | 1 |
続いて、1st PCR 産物を 3 反復プールし、AMPure XP (1:0.8) で精製、10 倍希釈後、下記条件で 2nd PCR を実行しました。総反応液量は 24 µL です。
| 項目 | 条件 |
|---|---|
| 2× KAPA HiFi HotStart ReadyMix | 12 µL |
| I5 primer (5 µM) | 1.4 µL |
| I7 primer (5 µM) | 1.4 µL |
| DDW | 7.2 µL |
| PCR template | 2.0 µL |
| 項目 | 温度 | 時間 | サイクル |
|---|---|---|---|
| 初期変性 | 95°C | 3 分 | 1 |
| 変性 | 98°C | 20 秒 | 12 |
| 伸長 | 72°C | 15 秒 | 12 |
| 最終伸長 | 72°C | 5 分 | 1 |
データ処理と種同定
FastQC と SUGAR で品質確認後、DynamicTrim.pl (Phred 10) で低品質末端を除去し、FLASH でペアエンドを結合(最小オーバーラップ 10 bp)しました。 さらに Perl スクリプトで不正長や不明塩基を除去し、TagCleaner でプライマー配列(最大 3 塩基ミスマッチ)を除去して FASTA 化しています。UCLUST によりデレプリケーションし、10 リード以上の配列を代表配列として保持し、10 リード未満の配列は 99% 以上一致する代表配列があれば同一とみなしました。
分類は Sarcopterygii のミトコンドリアゲノム(1,881 種、2016-03-15 時点)を基盤に構築したデータベースと、MitoFish に登録された魚類ミトコンドリア配列を統合したデータベースに対して BLASTN を実施し、同一率 97% 以上、E-value 1e-5 以下で最上位ヒットを種同定に用いています。 さらにアラインメント長/ミスマッチ数(例: 150/(1+1))の比を信頼性指標として算出しています。
Results and Discussion
MiBird-U は in silicoによる評価で高い一致率を示し、G/T ペアの許容下で MiBird-U-F は 410 種中 390 種(95.1%)、MiBird-U-R は 388 種(94.6%)と完全一致でした。
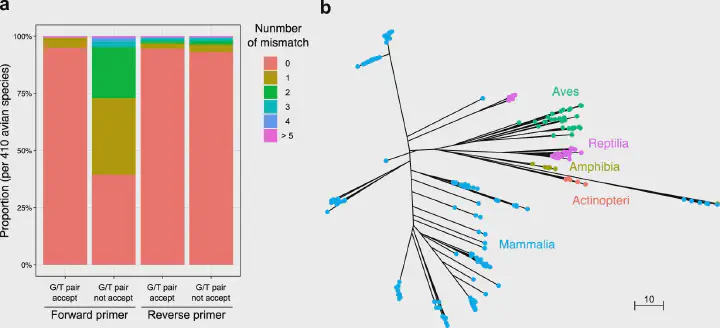
さらに 99.5% および 96.8% の種が 1 ミスマッチ以内であり、3’末端では MiBird-U-F で全種一致、MiBird-U-R でも 98.7% 以上が一致しています(Table 4 と Fig. 1)。編集距離による評価では 82,621 組中 82,177 組(99.5%)が 5 以上となり、種判別に十分な多型が含まれることが示されました(Table 5)。
Table 4. MiBird-U の塩基組成(407 種の鳥類配列)
MiBird-U-F
| Base | 1(G) | 2(G) | 3(G) | 4(T) | 5(T) | 6(G) | 7(G) | 8(T) | 9(A) | 10(A) | 11(A) | 12(T) | 13(C) | 14(T) | 15(T) | 16(G) | 17(T) | 18(G) | 19(C) | 20(C) | 21(A) | 22(G) | 23(C) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| A | 1 | 4 | 1 | 1 | 0 | 1 | 0 | 0 | 397 | 407 | 407 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 407 | 0 | 0 |
| C | 0 | 0 | 0 | 61 | 129 | 0 | 0 | 0 | 2 | 0 | 0 | 7 | 407 | 155 | 0 | 0 | 0 | 0 | 407 | 407 | 0 | 0 | 407 |
| G | 406 | 403 | 406 | 0 | 0 | 406 | 407 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 407 | 0 | 407 | 0 | 0 | 0 | 407 | 0 |
| T | 0 | 0 | 0 | 345 | 278 | 0 | 0 | 407 | 7 | 0 | 0 | 400 | 0 | 252 | 407 | 0 | 407 | 0 | 0 | 0 | 0 | 0 | 0 |
MiBird-U-R
| Base | 1(C) | 2(A) | 3(T) | 4(A) | 5(G) | 6(T) | 7(G) | 8(G) | 9(G) | 10(G) | 11(T) | 12(A) | 13(T) | 14(C) | 15(T) | 16(A) | 17(A) | 18(T) | 19(C) | 20(C) | 21(C) | 22(A) | 23(G) | 24(T) | 25(T) | 26(T) | 27(G) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| A | 0 | 407 | 0 | 406 | 0 | 0 | 0 | 2 | 0 | 0 | 0 | 407 | 0 | 1 | 0 | 407 | 407 | 0 | 0 | 0 | 0 | 406 | 0 | 1 | 0 | 0 | 0 |
| C | 407 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 406 | 0 | 0 | 0 | 0 | 407 | 406 | 404 | 0 | 0 | 1 | 0 | 5 | 1 |
| G | 0 | 0 | 0 | 0 | 407 | 0 | 407 | 405 | 407 | 407 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 405 | 0 | 0 | 0 | 406 |
| T | 0 | 0 | 407 | 1 | 0 | 406 | 0 | 0 | 0 | 0 | 407 | 0 | 406 | 0 | 407 | 0 | 0 | 407 | 0 | 1 | 3 | 0 | 2 | 405 | 407 | 402 | 0 |
対象 410 配列のうちプライマー領域欠失 3 種を除外し、407 種の塩基組成を集計。
Table 5. 編集距離の頻度分布
| Edit distance | 0 | 1 | 2 | 3 | 4 | >=5 | Total |
|---|---|---|---|---|---|---|---|
| Species | 27 | 50 | 67 | 113 | 187 | 82,177 | 82,621 |
| Genus | 10 | 23 | 40 | 80 | 157 | — | — |
primerTree による評価では鳥類の増幅だけでなく、哺乳類・両生類・爬虫類・魚類も増幅しうることが示され、鳥類に限定しない多分類群の同時検出にも使える設計であることが示唆されます。
組織 DNA では Table 2 に示した 22 種すべてで増幅に成功し、配列は DDBJ に登録されています。 動物園ケージ水では 16 種すべての対象鳥類が検出され、対象種のリード比率は 1.4-94.9% と幅がありました。
特に Steller’s sea eagle(オオワシ)、Capercaillie(ヨーロッパオオライチョウ)、White-naped crane(マナヅル)、Common crane(クロヅル)、Southern ground hornbill(ミナミジサイチョウ)などは 64.9-94.9% と高い比率で検出されましたが、Black-tailed gull(ウミネコ)、Humboldt penguin(フンボルトペンギン)、Snowy owl(シロフクロウ)などは 1.4-28.8% と低い割合にとどまっています。 これは水への接触頻度や行動の違いによると考えられ、環境DNAの検出量が行動や環境条件に左右されることを改めて示しています。
Ruddy shelduck(アカツクシガモ)の通り抜けケージでは、同居種である Lady Amherst’s pheasant(ギンケイ)、Temminck’s tragopan(ベニジュケイ)、Victoria crowned pigeon(オウギバト)、Mandarin duck(オシドリ)が同時に検出され、ケージ内の混在環境が反映されました。
非対象種の検出も多く、例えばオオワシの配列が他ケージで検出されるなど、飼育者の移動や風による DNA 移動、共用器具による混入など複数の要因が考えられます。 野外の池の水では調査地周辺で観察される鳥類 5 種が検出され、既知種以外の環境での有効性も示されました。 これらの結果は、視認調査が難しい状況での補完的手段として環境DNAメタバーコーディングが有効であることを示しています。
免責事項
十分注意は払っていますが、本記事の情報・内容について保証されるものではありません。また、本記事の利用や閲覧によって生じたいかなる障害についても責任を負いません。そして、本記事の情報は予告なく変更される場合がありますので、ご理解くださいますようにお願い申し上げます。
また、codexによるサポートを受けて記事を作成しています。