μCeta: 非標的脊椎動物の増幅を最小限に抑えた環境DNAメタバーコーディングのためのクジラ目特異的プライマーセット μCeta: A Set of Cetacean-Specific Primers for Environmental DNA Metabarcoding With Minimal Amplification of Non-Target Vertebrates
- 掲載誌: Environmental DNA (Wiley)
- DOI: 10.1002/edn3.70193
はじめに
クジラ目の環境DNA(eDNA)メタバーコーディングに特化した新規プライマーセット μCetaを開発し、非標的脊椎動物(魚類・ヒトなど)の増幅を抑えつつ種同定能力を高めることを目的とした研究です。
クジラ目は海洋生態系の指標種であり、保全上の重要性が高い一方で、目視や音響の調査はコストや条件に制約があります。 環境DNAは非侵襲的・低コスト・高感度という利点があるものの、従来の汎用プライマーでは魚類やヒトDNAが増幅されやすく、クジラ目の低濃度環境DNAが埋もれるという問題がありました。
本研究は、クジラ目に特化したプライマー設計により、非標的の増幅を抑えながら種解像度を確保することを狙っています。 さらに、水族館と沿岸という異なる環境を段階的に使うことで、設計から実地応用までの検証フローを示しており、他の海洋哺乳類マーカー設計にも応用可能な枠組みになっています。
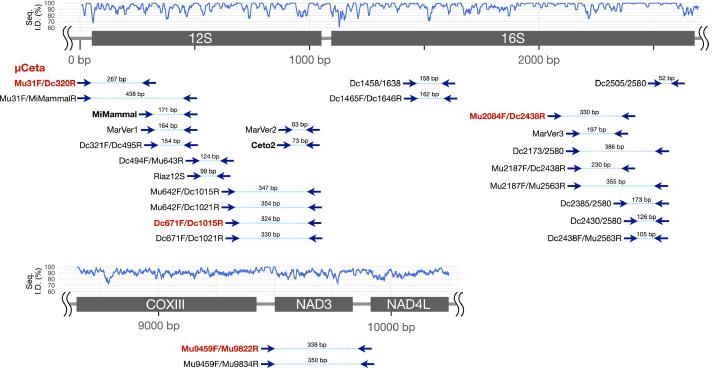
クジラ目のミトゲノム71種をもとに20の候補プライマーセットを設計し、in silico で特異性と種解像度を比較した上で、最も有望な4セットを実験にて検証しています。 候補領域は12S/16S rRNAやNAD3など保存領域を含む一般的にメタバーコーディング向きの領域を中心に選び、ヒトDNAの増幅回避を最優先条件として設計しています。 組織DNAで増幅性能を確かめ、水族館の循環水と香港沿岸の海水サンプルで実地検証することで、理論的な評価とフィールド適用の両面から性能を評価しています。
Methods
本研究は座礁個体や水族館で死亡した個体由来の組織試料を用い、沖縄美ら島財団、香港AFCD、Ocean Park Hong Kongの許可のもとで実施されています。 生体からの直接サンプリングは行っておらず、環境DNA採水も許可に基づく非侵襲的な手順で実施されています。 組織試料は沿岸で回収された個体と水族館保管個体に限定し、倫理面とコンタミ管理の両方に配慮した研究設計になっています。
プライマー設計
対象データはクジラ目71種(2亜目・11科・37属)のミトゲノムで、非標的の評価用にヒト・イヌ・ネコなどの哺乳類、ジュゴン・マナティーなど近縁分類群も含めています。
ミトゲノムはNCBI RefSeq(2023-07-11取得)から取得し、MAFFTのオンライン版でアライメントを行いました。 その上で候補領域20セットを抽出し、DECIPHER(DesignPrimers)と目視設計を併用して候補を作成しています。 DesignPrimersでは maxProductSize=500、numPrimerSets=30 を試し、12S/16S/NAD3で設計領域を絞り込んでいます。
設計条件はプライマー長19–28 bp、GC 40–60%、Tm差を小さく、アンプリコン長<450 bpとし、特にヒトDNAの増幅を避けることを重視しています。
in silicoでの評価
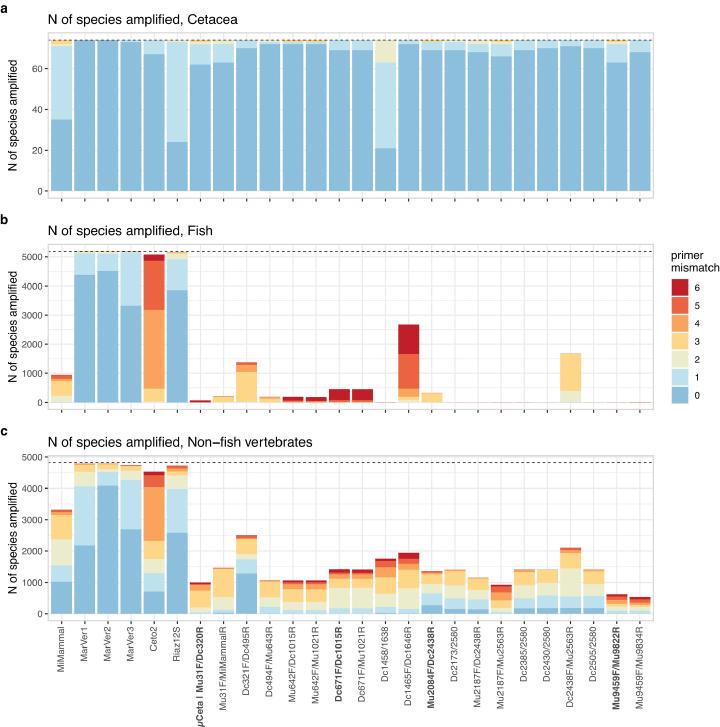
in silicoでの評価では、10,855分類群・36,250配列(クジラ74、非クジラ哺乳類2378、鳥1556、爬虫類700、両生類733、魚5411、その他1)を対象に、USEARCHの search_oligodb / search_pcr でミスマッチ数や増幅種数を評価しました。 MiMammal、MarVer1/2/3、Ceto2、Riaz12Sなど既存プライマーも比較対象に含め、候補群の非標的脊椎動物の回避性能を相対評価しています。
USEARCHの search_oligodb は maxdiffs を最大4まで、search_pcr は maxdiffs を最大3まで検討し、minamp 30・maxamp 2000を設定して増幅可否を判定しています。 増幅種数・アンプリコン長・編集距離(配列間の最小編集数)を並列に比較することで、特異性と判別力のトレードオフを可視化しました。
この評価では、アンプリコン長の分布も重視され、推定長は概ね100–500 bpの範囲に収まることが確認されています。 ショートリードのIlluminaでシーケンス可能である一方、Mu31F/MiMammalRのように300 bpペアエンドが必要な候補は機材制約が生じるため、フィールドでの使用のしやすさも選定基準に組み込まれています。 非標的の中でもヒトDNAの非増幅が重視され、沿岸域でのコンタミネーションリスクを前提に設計されています。
実証評価: 組織DNAと水試料
実証評価は、座礁個体や水族館個体由来の組織DNA(19種)と、水族館水槽水・香港沿岸の海水の3系統で行われました。 組織DNAは2亜目・5科の19種で、S.chinensis以外は沖縄美ら島財団、S.chinensisはOcean Park Hong Kongの保管試料が用いられています。
水族館試料は沖縄の7プール(2循環区画)から1–2 L採水し、プール容量は1200–1750 m3の大型プールから400–500 m3の小型プールまでの幅があります。 プール試料は計9点とフィールドネガティブコントロール1点の計10点がサンプリングされ、香港沿岸はP1で表層500 mL、P2で表層・亜表層1 Lずつの採水に加えて、P3のインド太平洋ザトウイルカ観察地点で500–1500 mLのリール度を2点採水しています。 P1は2023年2月、P2は2023年7月、P3は2024年7月の採水です。
ろ過は0.45 μmのSterivexを用い、RNAlater 2 mLを添加してクーラーボックスで保冷後、-20°Cで保管しています。 抽出はFukuzawa et al. 2023に基づく修正版で、Buffer ATLとProteinase Kを用いた溶解後にDNeasy Blood & Tissueで精製し、100 μLで溶出しました。 抽出ネガティブコントロールも各処理で組み込み、プール試料は「Main Pool」「Main Show Pool」の2点のみ複数抽出をプールして7サンプルとしています。
ライブラリ調製は2-step PCRで、Platinum SuperFi IIを用いた1st PCR(Illuminaシーケンスプライマー付き)後にAMPure XP精製、2nd PCRでインデックス付与を行っています。 PCR ネガティブコントロールも複数組み込み、コンタミネーションを監視しています。フィールドポジコンは μCeta のみを対象に、タグ付きプライマーのearly-pooling法を採用し、ExoSAP-IT Expressで処理しています。 MiMammalとCeto2の検証ではiSeq 100(2×150 bp)を用い、PhiXを30%添加してシーケンスしています。
解析はDADA2でASVを作成し、removeBimeraDenovoでキメラ除去後、必要に応じてmergeSequenceTablesで統合しています。 分類同定はQCauto(Claident)とdada2のassignSpeciesに加え、手動BLASTで補強する保守的な運用で、フィールドポジコンは97%でOTU化してから同定しています。 サンプル数は4プライマーで各16サンプル、フィールドポジコンは6サンプル、MiMammal/Ceto2は各12サンプルという設計です。
分類同定ではQCautoが「近傍配列が同じ分類群に一致する場合のみ同定する」という保守的な判定を行うため、誤同定を抑えつつ未同定が増える設計です。 水族館試料と香港試験試料は近縁種やハイブリッドを含み得るためASVベースで判定し、フィールドポジコンはOTU化してから同定しています。 補助的な比較としてMiMammalとCeto2もiSeq(2×150 bp)で試験され、PhiX 30%添加でシーケンスしています。

実証対象として選ばれた4セットは、12S rRNA領域の μCeta と Dc671F/Dc1015R、16S rRNA領域の Mu2084F/Dc2438R、NAD3領域の Mu9459F/Mu9822R で、対象領域長は267–338 bpに揃えられています。 配列とGC比はTable 1にまとめられており、μCetaが最短ながら判別力を確保できる設計になっています。
Table 1: 実証試験に用いたプライマーセット
| Primer set | Region | Forward (5’-3') | Reverse (5’-3') | Target (bp) | GC% (F/R) |
|---|---|---|---|---|---|
| Mu31F/Dc320R (μCeta) | 12S rRNA | GACACTGAAAATGTCTAGATGG | TYAATCGTATGACCGCGGTG | 267 | 40.9 / 52.5 |
| Dc671F/Dc1015R | 12S rRNA | GCTACTYCAGTCTATATACC | CACACYTTCCRGTAYGCTTACC | 324 | 42.5 / 52.3 |
| Mu2084F/Dc2438R | 16S rRNA | ATGAAYGGCCACACGAGGGTTTTA | TGTCCTGATCCAACATCGAGG | 330 | 47.9 / 52.4 |
| Mu9459F/Mu9822R | NAD3 | CTGACTTCCAATCAGTTRGTTTCGG | CATTCTARRCCYTYTTGRG | 338 | 46.0 / 44.7 |
Note
対象領域長は Delphinus capensis のミトゲノムに基づく
Results
各種要点のみ記載しています。
in silico評価
20の候補のうち、ヒトDNAに4ミスマッチ以上となるセットが10組あり、候補プライマー群全体として非標的脊椎動物を回避する設計となっています。加えて、候補プライマーセットは魚類・鳥類・爬虫類・両生類に対してもミスマッチが多く、既存の汎用プライマーより非標的脊椎動物の増幅を抑える傾向が示されています。
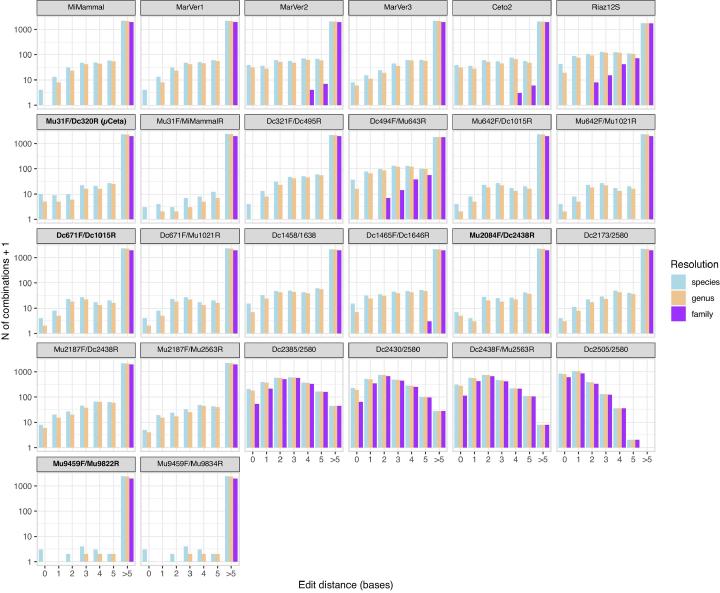
一方で、短い領域ほど種判別能が低下し、Ceto2やRiaz12Sでは同一配列が多いという弱点が確認されています。 編集距離の分布を踏まえ、非標的回避と判別能の両面で良好かつ退化塩基が少ない μCeta、Dc671F/Dc1015R、Mu2084F/Dc2438R、Mu9459F/Mu9822R の4セットが実証対象に選定されました。
種判別能の評価では、短い領域ほど編集距離0のペアが増え、種レベルの分解能が不足することが可視化されています。逆に長すぎる領域はシーケンス負荷が上がるため、12S/16Sの300 bp前後という設計は「判別力と実務性の折衷点」として妥当であることが示されています。
組織DNAの増幅
組織DNAの実験では、μCeta と Mu2084F/Dc2438R が19種すべてで増幅に成功し、Dc671F/Dc1015R は1種、Mu9459F/Mu9822R は4種で増幅に失敗しました。 Dc671F/Dc1015Rの失敗はオキゴンドウ(Globicephala macrorhynchus)で、Mu9459F/Mu9822RはG. macrorhynchus、Kogia sima、Kogia breviceps、Mesoplodon ginkgodensで失敗しています。 対象には14–15年保存の組織も含まれるため、退化塩基の多さとDNA劣化が重なった可能性が示唆されます。Table 2 の一覧からも μCeta が最も安定的 と判断できます。
Table 2: 組織DNAでの増幅結果(アクセッション番号)
Note
aは部分配列、bはLC867742/LC867743が追加登録、cはLC867746/LC867747が追加登録。
水槽・沿岸試料での環境DNA検出
水族館サンプルでは、飼育されている5種を4プライマーで概ね検出できましたが、μCetaのみが全プールで種レベル同定に成功しました。 Pseudorca crassidensとTursiops truncatusは全プライマーで検出され、T. aduncusは μCeta と Mu9459F/Mu9822R で同定できた一方、Dc671F/Dc1015R や Mu2084F/Dc2438R では「Unidentified Delphinidae」にとどまる例が多く、近縁種の分解能が不足しやすい傾向が確認されています。 Feresa attenuata は Mu9459F/Mu9822R を除く3プライマーで検出され、Steno bredanensisは全プライマーで検出されました。一方、循環区画内では存在しない種が検出される例もあり、水流による環境DNAの移動の影響が示唆されました。
シーケンス概要としては、4プライマー・64サンプルから3,332,270リードを取得し、Q30は92.08%でした。 プライマー別のリード数は μCeta が902,908、Dc671F/Dc1015Rが781,005、Mu2084F/Dc2438Rが782,716、Mu9459F/Mu9822Rが865,741で、DADA2後に2,572,852リード(77.21%)となっています。 ネガティブコントロールではMu2084F/Dc2438Rの抽出ネガティブコントロールで2,650リード(平均の2–3%)が出たものの、大半がヒト由来でμCetaの水槽のネガティブコントロールは712リード(平均の0.7%以下)、PCR陰性は0.1%未満と報告され、コンタミは重大ではないと判断されています。
非存在種の検出については、Dc671F/Dc1015Rでミンククジラ(Balaenoptera acutorostrata)が最大0.76%で検出された例があり、その影響は小さいとされています。 さらにTursiops australisなどの稀なASVが除去されていますが、餌魚に付着したDNAなどの外部要因が残留する可能性は否定できず、水槽実験であっても混入DNAに関する評価が必要であることが示されています。
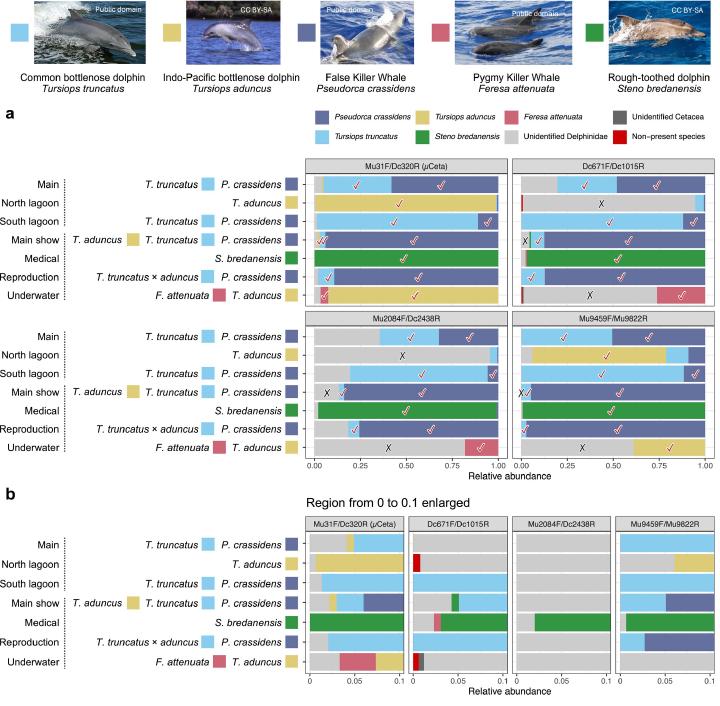
追加の比較として、MiMammalとCeto2も水族館サンプルおよび香港試験サンプルで簡単に検証されています。 iSeq(2×150 bp)で2,406,398リード(Q30=95.80%)を取得し、DADA2後に2,212,982リードが残りましたが、Ceto2は73 bpと短いため種解像度が低く、種名が付与できたのは2種にとどまるなど、候補プライマー群の優位性が補強されています。
香港沿岸での実地検証
香港沿岸の採水サンプル(P1/P2)では、ターゲットと非ターゲットの増幅傾向を評価し、フィールドポジコン(P3)では μCeta のみを用いてフィールドでの検証を行っています。 2024年7月のフィールドポジコンでは、インド太平洋ザトウイルカ(Indo-Pacific humpback dolphin; Sousa chinensis) の環境DNAを検出しました。 採水地点と個体の距離が約30 mであった点を踏まえても、μCetaが実環境で十分な感度を持つことが示され、魚類やヒトなど非標的の増幅を抑えながら狙ったクジラ目の検出が可能であることが確認されています。
一方で、沿岸の検証は地点数が限られるため、広域分布や季節変動の推定には今後の反復調査が必要です。μCetaは検出精度の底上げに有効ですが、空間・時間スケールを拡張した運用設計が次の課題になります。
まとめ
本研究は、クジラ目に特化したプライマーを設計・in silico評価・フィールドでの検証までを実施し、特に、μCeta(12S rRNA, 267 bp) は組織DNAと最水サンプルの双方で安定的に機能し、他の候補よりも種解像度が高いことが確認されました。
種同定の精度は参照配列の網羅性に依存するため、対象海域での参照DBの更新が継続的に必要です。クジラ目はミトゲノム情報が比較的整備されているとはいえ、地域集団や近縁種の分解能はDBの質に左右されるため、μCetaの有効性を最大化するにはDB整備とセットで運用することが重要になります。
また、in silico評価から「短すぎる領域は判別能が落ちる」ことが明確に示され、増幅のしやすさと種解像度のバランスが重要であることを再確認させる結果でした。水族館の水槽サンプルでの非存在種の検出は、環境DNAが循環水で移動することを示し、実地調査では水理条件を踏まえた解釈が必須であることを示唆します。
実運用では、採水量やろ過条件、ネガティブコントロールの運用が検出結果の信頼性に直結します。本研究のように複数のネガティブコントロールを組み込む設計は、低濃度環境DNAを扱うクジラ目調査に特に有効です。また、環境DNAは検出の空間代表性に限界があるため、目視・音響・衛星観測など既存手法との併用が現実的で、μCetaはそれらを補完する高感度ツールとして位置づけられます。
μCetaはクジラ目のeDNAメタバーコーディングにおいて、非標的種の増幅を抑えつつ種レベルの解像度を確保する有力なプライマーであり、沿岸域でのクジラ目モニタリングに現実的な選択肢となります。 特に、ヒトDNAや魚類DNAを回避しつつ、インド太平洋ザトウイルカを検出できた点は多様性評価や定期モニタリングなどで価値が高く、今後の保全モニタリングへの応用が期待されます。
免責事項
十分注意は払っていますが、本記事の情報・内容について保証されるものではありません。また、本記事の利用や閲覧によって生じたいかなる障害についても責任を負いません。そして、本記事の情報は予告なく変更される場合がありますので、ご理解くださいますようにお願い申し上げます。
また、codexによるサポートを受けて記事を作成しています。